آمونیاک
آمونیاک
آمونیاک (انگلیسی Ammonia) از تجزیهٔ مواد آلی ازت دار همچون اوره ادرار بهدست میآید.
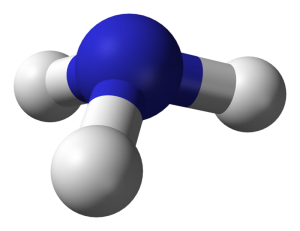
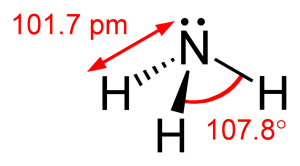
مولکول آمونیاک از ترکیب یک اتم نیتروژن و سه اتم هیدروژن با فرمول شیمیایی NH3 تشکیل شدهاست.
مولکول آمونیاک یک مولکول قطبی است که میتواند با خودش و بسیاری مولکولهای دیگر، پیوند هیدروژنی برقرار نماید.
این ماده طبق نظریههای اسید و باز برونستد-لوری و لوویس، یک ترکیب بازی محسوب میشود.
pH محلول آبی آن از ۷ بیشتر است که این واقعیت را آشکار میسازد.
جهت مشاوره با کارشناسان ما تماس حاصل فرمایید.
نمکهای آمونیاکی
نمکهای آمونیاکی که از تقطیر زغال سنگ بدست میآیند، بر دو نوعند:
- نمکهای فرار مانند کربنات آمونیوم CO3(NH4)2 و سولفیدرات SHNH4 و S(NH4)2 که بهآسانی بوسیله بخار آب برده میشوند.
- نمکهای ثابت و غیر فرار مانند کلرید آمونیوم NH4Cl و هیپوسولفیت S2O3(NH4)2 و غیره که بوسیله باز غیر فراری مانند آهک تجزیه میگردند.
ضمنا باید متذکر شد، آمونیاکی که از تقطیر یک تن زغال سنگ حاصل میشود، طبعا با مقدار ازت موجود در زغال متغیر است و این مقدار بین 1,4 کیلوگرم تا 4,6 کیلوگرم نوسان دارد و بهندرت در بعضی از انواع زغال سنگها این مقدار به 7,2 کیلوگرم میرسد.
معمولا هرگاه عمل تقطیر زغال سنگ را در مجاورت 2,5 درصد آهک انجام دهند، بهره آمونیاک تا 20 درصد افزایش نشان میدهد و به هر صورت ، آمونیاک و کلیه ترکیبات آمونیاکی را که در بالا نام بردیم، میتوان در دستگاههای خنک کننده از قطرانهایی که همراه آنها میباشند، جدا کرد و اصطلاح صنعتی این قبیل محلولهای آمونیاکی را آبهای آمونیاکی مینامند که آنها را ابتدا در ستونی تقطیری وارد میکنند.
سپس تحت تاثیر شیر آهک قرار میدهند و در آنجا آمونیاک و املاح فرار آنها بوسیله بخار آب برده میشوند.
در حالیکه املاح غیر فرار تحت تاثیر شیر آهک ، تجزیه و به آمونیاک تبدیل میگردند.
فرآیند تولید
در دهه اول قرن بیستم با توجه به گسترش استفاده از کودهای نیتروژن دار و استفاده گسترده از Ammonia در تولید آن ها ، یافتن راهی برای تولید بهینه این ماده از دغدغه های اصلی جهت تولید کود نیتروژنه بود.
روش های مختلفی برای این امر ارائه شدند که به دلیل مشکلات عملیاتی و یا هزینه زیاد از لحاظ اقتصادی به صرفه نبودند ، در این میان هابر توانست با ارائه روشی عملی و به صرفه اماکان تولید آمونیاک در مقیاس بزرگ صنعتی را فراهم کند.
روش هابر
روش هابر برپایه سنتز کاتالیستی آمونیاک از گازهای هیدروژن و نیتروژن بود. هابر در سال 1905 با استفاده از دمای بالا (500 °C) ، فشار بالا (150 تا 200 اتمسفر) و یک کاتالیست آهنی توانست این دو گاز تقریبا غیرفعال را ترکیب کرده و آمونیاک را تولید کند. همکاری هابر و بوش باعث شد که در سال 1913 سنتز آمونیاک در فشار بالا محقق شود.
اولین واحد تجاری برای تولید این ماده توسط شرکت BASF در آلمان راه اندازی شد که ظرفیت تولید 30 تن در روز را داشت. امروزه نیز تولید آمونیاک بر همان پایه روش هابر – بوش استوار است ، هرچند که این روش در طول سالیان شاهد بهبودها و به روز رسانی های زیادی بوده است.در یکی از این روش ها واکنش در دمای 500 درجه سانتیگراد و فشار 200 اتمسفر انجام می گیرد ، در هر بار عبور گازها تنها بین 10 تا 18% از آمونیاک مورد انتطار تولید می شود.برای حل این مشکل جریان گازهای برگشتی در یک سیکل دوباره به راکتور واکنش برمیگردند و با این کار می توان به 97% آمونیاک مورد نظر دست پیدا کرد.
واحد های تولیدی امروزی 6 مرحله اصلی دارند که عبارتند از :
سولفور زدایی گاز طبیعی ، ریفورمینگ کاتالیستی بخار ، تغییر کربن مونو اکسید ، حذف گاز کربن دی اکسید ، متانیشن و سنتز آمونیاک. دیاگرام این فرآیند را می توان در شکل زیر مشاهده کرد.
سرگذشت
رومیها آمونیوم کلرید را به عنوان پول و سپرده استفاده میکردند.
آنها سنگ آمونیوم را از مکانی به نام پرستشگاه ژوپیتر یا همان لیبی امروزی جمعآوری میکردند.
اما نخستین بار به شکل نمک آمونیاک توسط شیمیدان ایرانی جابر بن حیان (انگلیسی: Geber) در قرن ۸ شناخته شد.
جدول خواص فیزیکی
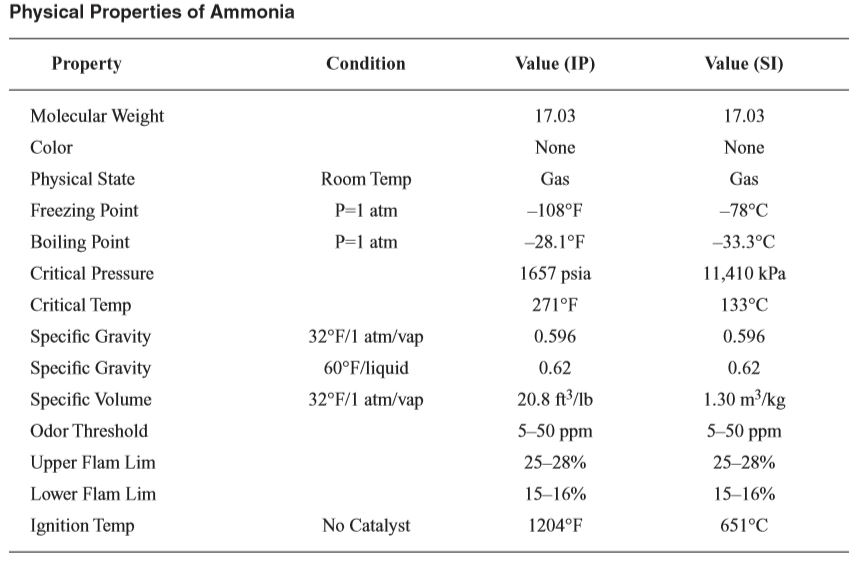
جدوا خواص شیمیایی آمونیاک
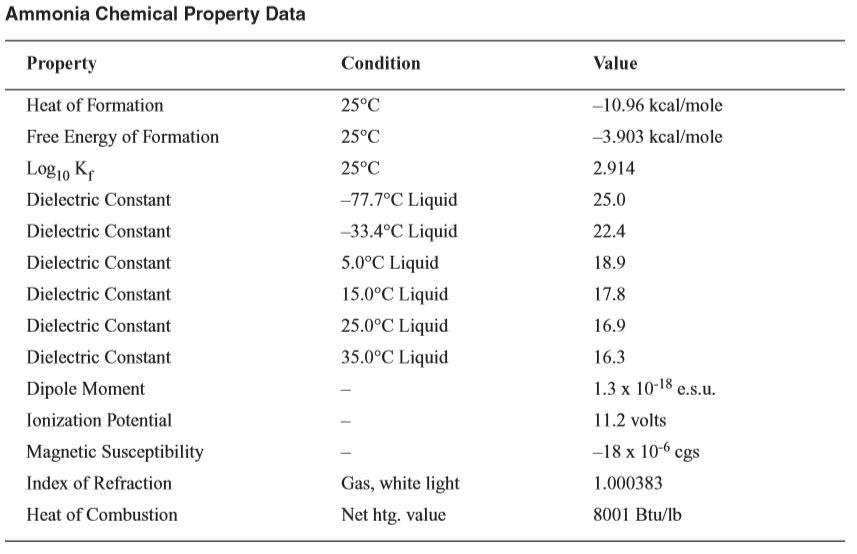
کاربرد
این ماده در تهیهٔ کودهای شیمیایی، یخ سازی، اسید نیتریک، سایر ترکیبات نیتروژنه، مواد منفجره و نگهداری از مواد غذایی مورد استفاده قرار می گیرد.
تعدادی از کاربرد های دیگر
- کاهشگر nox در سیستم کاتالیست کاهنده
- مورد استفاده در تولید نیتریک اسید و آمونیوم نیترات
- کاربرد در صنعت رنگ
- کاربرد به عنوان سوخت و مشتقات سوختی
- کاربرد در تصفیه آب
- مصارف خانگی صورت محلول رقیق به عنوان ماده سفید کننده
خطرات بهداشتی
موجب تحریکات سیستم تنفسی ، پوست و چشم شده و در اثر مواجهه با حجم زیاد این گاز به ریهها آسیب رسانده و سبب مرگ شود.
در صورت تماس با آمونیاک مایع ، محل تماس دچار سوختگی شدید می گردد.
شرکت دانش پژوهان شیمی نماینده فروش محصولات شرکت مرک و سیگما آلدریچ آلمان.
شرایط نگهداری
باید در جای خشک و خنک با تهویه مناسب به دور از اشعه آفتاب و گرما و منابع محترق و مواد آتش گیر انبار شوند.
سیلندرهای این ماده بدور از آسانسور راه روها انبار شود. توصیه می شود مخازن بزرگ آمونیاک در هوای آزاد و زیر سایه نگهداری شوند.
خطرات آتش سوزی و انفجار
آمونیاک ، گازیست قابل اشتعال و حدود اشتعالش 16 تا 25 درصد حجمی گاز آمونیاک در هوا میباشد. حضور مواد نفتی و دیگر مواد قابل اشتعال ، خطر حریق را افزایش میدهند. محلول غلیظ اکسید نقره از محلول آمونیاک حل شده و تولید فولمینات نقره به فرمول CNOAg مینماید که ماده ای شدیداً قابل انفجار است.
همچنین گاز آمونیاک در اثر حرارت از 400 درجه به بالا تجزیه شده ، تولید هیدروژن مینماید.
خطرات بهداشتی
سبب تحریکات سیستم تنفسی ، پوست و چشم شده و با آسیب رساندن به ریهها در اثر مواجهه با حجم زیاد این گاز میتواند سبب مرگ شود. در صورت تماس با آمونیاک مایع ، سوختگی شدید در محل تماس ایجاد میگردد. آستانه مجاز مواجهه با آن ، ppm 50 است و جهت کمکهای اولیه ، قسمتهای آلوده سطح بدن را با آب و صابون شسته و چشمها را نیز با آب فراوانی شستشو داد و به پزشک مراجعه نمود.
طریقه اطفاء حریق
در صورتیکه سیلندر گاز آمونیاک مشتعل شد، نباید شعله آن را خاموش نمود، مگر اینکه قبلاً بتوان جریان گاز را قطع کرد.
در حین عملیات اطفاء ، باید سیلندرهای حاوی گاز آمونیاک را با آب خنک نمود.
از پودر شیمیایی خشک یا گاز کربنیک یا آب بهصورت اسپری جهت اطفاء میتوان استفاده نمود.
به هنگام عملیات باید از لباس کاملاً ایمن و سیستم حفاظتی دستگاه تنفس استفاده کرد.

کمک های اولیه
تماس تنفسی : فرد مصدوم را به هوای آزاد ببرید و اگر تنفس به سختی انجام می شد به فرد دستگاه اکسیژن وصل کنید و به پزشک مراجعه کنید.
تماس پوستی : سریعا موضع را با آب ولرم و به آرامی شستشو دهید. در صورت سوختگی یا سوزش به پزشک مراجعه کنید.
تماس چشمی : سریعا چشم را با مقدار زیادی آب ولرم به آرامی و به مدت 10 تا 20 دقیقه شستشو دهید چشمها را با نوار استریل بسته و به پزشک مراجعه کنید.
بلع و گوارش : به مصدوم شیر یا آب بدهید و اجازه دهید از طریق تهوع، تخلیه گوارشی شود در صورتی که مصدوم هوشیار نباشد از برگرداندن محتویات معده بصورت اجباری اجتناب کنید.
طریقه نگهداری و حمل ونقل
آمونیاک باید در سیلندرهای استیل نگهداری و توسط تانکرهای مخصوص آن حمل گردد. باید سعی نمود از رسیدن تنشهای فیزیکی و حرارت زیاد به ظروف محتوی آمونیاک جلوگیری شود. انبار و محل نگهداری آن باید مقاوم در برابر حریق بوده و دارای سیستم اعلام و اطفاء اتوماتیک باشد.
آمونیاک باید جدا از موادی چون گازهای اکسید کننده ، کلر ، برم ، ید و اسیدها نگهداری شود.
بازار جهانی
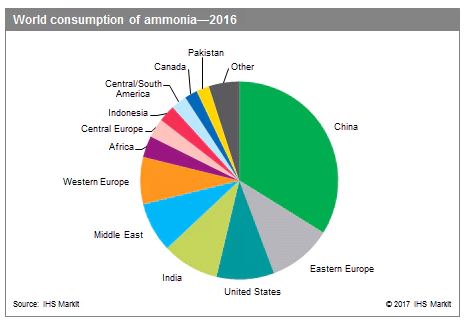
ارزش بازار جهانی Ammonia در سال 2016 حدود 48.65 میلیارد دلار بوده و انتظار می رود که تا سال 2025 به مقدار 76.64 میلیارد دلار برسد. مطابق پیش بینی ها، همچنین انتظار می رود که تا پایان دوره پیش بینی شده، با رشدی حدود 5.3 درصد از سال 2017 تا سال 2025 دست پیدا کند. منطقه آسیا پاسفیک در سال 2016 بر این بازار چیره شده و پیش بینی ها، سریع ترین نرخ رشد در این بازار را برای این ناحیه متصور می باشند.
منابع : دانشنامه رشد ، مبتکران شیمی ، تهران اسید ،
Visits: 10
